Tumeurs | Osseuses
Jeune fille de 8 ans. Bilan de gonalgies inflammatoires.
Image A: radiographie de genou de face. Lacune épiphysaire distale arrondie de la fosse intercondylienne.
Image B: Scanner réalisé sans injection de produit de contraste avec reconstructions en coupes sagittales (B.1), axiales (B.2) et coronales (B.3). Lacune osseuse bien limitée du toit de l’échancrure intercondylienne postérieure, réalisant une petite effraction de la corticale postérieure, sans réaction périostée. Il existe de fines calcifications au sein de la lacune. Condensation périphérique dégressive d’allure inflammatoire autour de la lésion.
Image C: IRM réalisée en coupes axiales en séquences T1 (C.1), axiales DP-FatSat (C.2), sagittales DP FatSat(C.3). Lésion hétérogène en signal intermédiaire T1 et T2, avec présence de microkystes, aux contours lobulés. Réaction inflammatoire importante des parties molles (synovite postérieure) et de la médullaire osseuse adjacente.
Diagnostic anatomo-pathologique: Chondroblastome.
Discussion:
Tumeur bénigne rare (<1% des tumeurs osseuses primitives).
Terrain: 2 hommes/1 femme. Age de survenue entre 5 et 25 ans.
Localisation: atteinte des os longs, épiphysaire ou apophysaire (genoux, têtes fémorales, têtes humérales: 75% des cas), puis tarse, acétabulum et patella.
Atteinte épiphysaire ou épiphyso-métaphysaire.
Clinique: douleurs de rythme inflammatoire, simulant une arthrite, parfois avec épanchement articulaire.
Caractéristiques en imagerie:
Ostéolyse géographique à contours arrondis, lobulés ou ovalaires.
Limites nettes avec liseré d’ostéosclérose et parfois condensation dégressive de type inflammatoire.
Matrice cartilagineuse avec calcifications intra lésionnelles.
La corticale osseuse peut être rompue.
En IRM, le signal est intermédiaire en séquence T1 et T2, sans signal « myxoïde » en hyper signal T2 des lésions cartilagineuses, en raison de sa cellularité élevée.
La réaction inflammatoire locale peut être très importante, pouvant faire simuler une arthrite ou une ostéite.
Référence:
Tumeurs osseuses et pseudo-tumeurs osseuses, imagerie rhumatologique et orthopédique, Laredo et al.
Bilan d’une lacune phalangienne indolore soufflant la corticale de découverte fortuite.
Lésion centro médullaire de P2 (![]() ), bien limitée, soufflant la corticale (
), bien limitée, soufflant la corticale (![]() ).
Elle est hypointense en T1, hyperintense en T2 et se rehausse
essentiellement en périphérie traduisant une matrice cartilagineuse.
Absence de signes évoquant des images calciques.
).
Elle est hypointense en T1, hyperintense en T2 et se rehausse
essentiellement en périphérie traduisant une matrice cartilagineuse.
Absence de signes évoquant des images calciques.
IRM de l'humérus (a: coronal DP FS, b: sagittal DP FS, c: sagittal T1).
La tumeur est formée de lobules cartilagineux en hyposignal T1, hypersignal T2 franc, pseudo liquidien (à l'exception des zones calcifiées), cerclés par des septas en hyposignal.
Absence d'oedème péri-lésionnel
Persistance de moelle graisseuse en T1 considérée comme un élément en faveur d'un chondrome (voire chondrosarcome de grade 1) et contre un chondrosarcome de grade 2 ou 3.
Scanner (a: coronal, b: sagittal, c: axial) : Lacune centrale, bien limitée, sans condensation périphérique (1B), aux contours arrondis sans encoche endostée et siège de calcifications de type cartilagineux en grains grossiers irréguliers avec "aspect en pop corn".
"Imagerie rhumatologique et orthopédique; Tumeurs osseuses et pseudo tumeurs osseuse" Laredo
Homme de 31 ans sans antécédent particulier. Bilan de masse et douleur costale postéro-latérale droite.
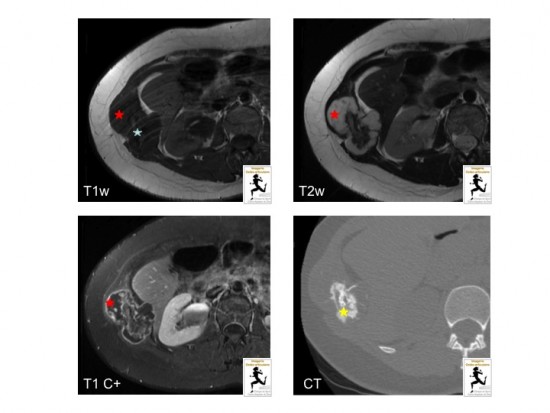
IRM (axial T1; axial T2; axial T1 après injection de gadolinium avec saturation de la graisse) ; TDM ( Scanner en fenêtre osseuse).
Masse centrée sur la 9ème cote droite au niveau de la jonction ostéo-cartilagineuse (étoile bleue), hétérogène avec matrice cartilagineuse (étoile jaune : calcifications arciformes centrales en TDM ; étoile rouge : matrice cartilagineuse en hyposignal T1 et franc hypersignal T2 de plus de 2 cm d'épaisseur) avec importante prise de contraste périphérique. Cet aspect évoque en premier lieu une tumeur cartilagineuse de haut grade de type chondrosarcome costal.
Lin JR et al. Primary malignant bone neoplasm: a case report of dedifferentiated chondrosarcoma in the rib and review of the literature, Chin J Cancer, 2010.
Garçon de 14 ans, bilan de sciatique droite.
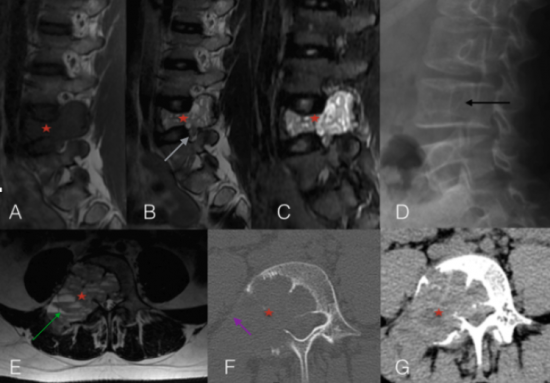
IRM du rachis lombaire en coupes sagittale T1 (A), T2 (B), T2 STIR (C) et axiale T2 (E) montrant une lésion expansive bien limitée de 5 cm centrée sur le pédicule L4 droit (étoile rouge). Elle est constituée de multiples logettes kystiques (flèche verte) contenant des niveaux liquide-liquide en faveur du caractère hémorragique. La lésion est responsable d'un élargissement du pédicule aux dépends de l'espace inter disco articulaire et du foramen L4-L5, avec compression de la racine L4 à son émergence (flèche grise) et dans son trajet pré-foraminal.
La TDM non injectée en coupe axiale centré sur L4 en fenêtre osseuse (F) puis molle (G) retrouve un pédicule élargi par une lésion lytique, cernée par endroits d'une coque périostée (flèche violette) témoignant d'une agressivité intermédiaire.
La radiographie initiale (D) montrait une lyse du pédicule transverse droit de L4 (flèche noire).
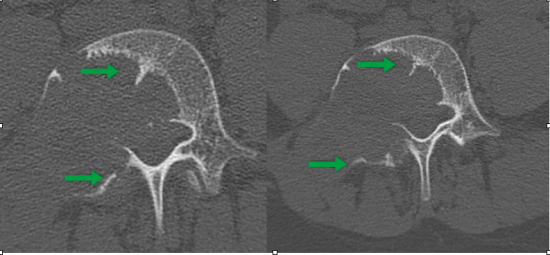
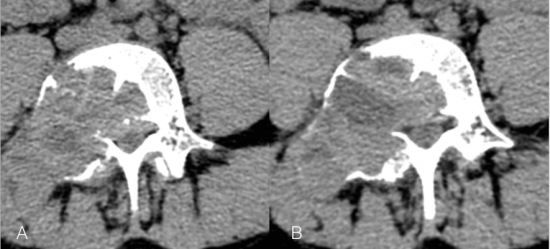
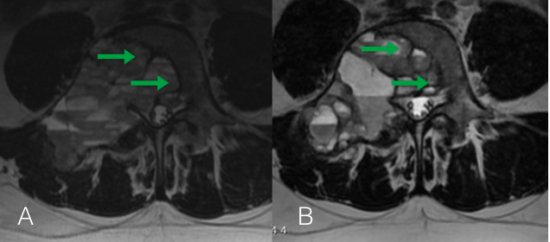
Suivi sous traitement par biphosphonates à 4 mois d'intervalle: le TDM et l'IRM en séquences T2 permettent de retrouver un début d'ostéocondensation périphérique de la lésion (flèches vertes), qui est stable en taille.
L'aspect dès l'IRM est typique de celui d'un kyste osseux anévrysmal (KOA). Il s'agit d'une lésion kystique et hémorragique bénigne atteignant principalement des patients jeunes de 5 à 20 ans, avec une prédominance féminine. Ils peuvent être primitifs mais la fréquence des formes secondaires impose la recherche d'une lésion sous-jacente, et notamment dans cette tranche d'âge un ostéoblastome, un chondroblastome ou plus rarement un ostéosarcome. Ils pourraient également être post-traumatiques. Chez l'adulte il faut rechercher une tumeur à cellules géantes, un fibrome chondromyxoide, une dysplasie fibreuse.
Le KOA peut toucher n'importe quelle région, mais essentiellement la métaphyse des os longs (67%). Au niveau rachidien, la localisation préférentielle est l'arc postérieur des vertèbres cervicales ou lombaires.
Les radiographies standard montrent une lésion ostéolytique excentrée bien limitée. Il existe un amincissement cortical périphérique et la formation de septas centraux donne un aspect en "bulles de savon".
L'IRM permet de mettre en évidence les niveaux liquide-liquide dans la lésion et surtout d'apprécier l'extension dans les tissus mous adjacents.
Le principal diagnostic différentiel est l'ostéosarcome télengiectasique, justifiant la réalisation d'une biopsie. Elle permet également de rechercher une lésion sous-jacente (KOA secondaire).
Le traitement chirurgical reste la référence mais, compte tenu de son caractère délabrant, il peut être délaissé au profit d'un traitement médical par biphosphonates visant à obtenir une sclérose de la lésion.
Bone cysts: unicameral and aneurysmal bone cyst. Mascard et al., Orthopaedics and traumatology: surgery and research 101 (2015) S199-S127
Gebauer GP, Farjoodi P, Sciubba DM, et al. Magnetic resonance imaging of spine tumors: classification, differential diagnosis, and spectrum of disease. J Bone Joint Surg Am 2008; 90: 146-62.
Patient de 45 ans, odeur gênante intermittente du 3ème doigt de la main gauche.
Antécédent de traumatisme de l’extrémité distale de ce doigt par écrasement (coup de marteau) il y a 20 ans.
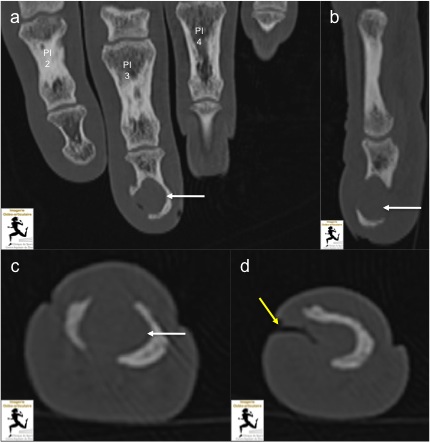
TDM de la main gauche centrée sur le 3ème rayon en coupe coronale (a), sagittale (b) et axiale (c et d) : Plage lytique arrondie bien circonscrite de la houppe de la phalange distale du 3ème rayon (flèche blanche), centimétrique, avec lyse du versant dorsal et latéral de la corticale adjacente. Absence de calcification ou de trabéculations intra-lésionnelles. Il s’y associe une image de « pertuis » sous la forme d’une image linéaire gazeuse étendue depuis le revêtement cutané jusqu’au niveau de la lésion, au niveau de son bord radial (flèche jaune).
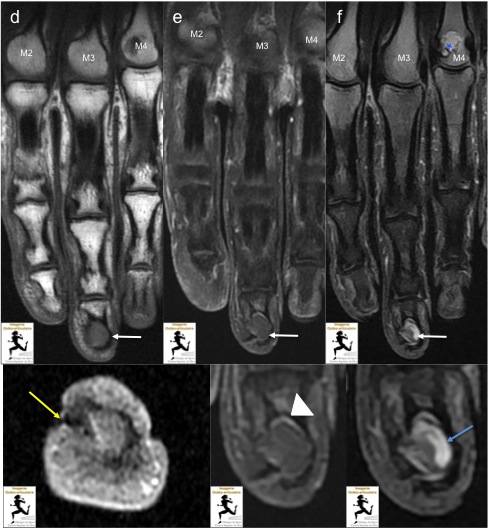
IRM de la main gauche centrée sur le 3ème rayon en coupes coronales pondérées T1(a) , T1 avec injection de gadolinium et saturation de graisse (b) et DP avec saturation de graisse : On retrouve la plage lytique de la houppe de la phalange distale du 3ème rayon (flèche blanche), présentant un signal T1 intermédiaire avec minime rehaussement périphérique (tête de flèche) et un hypersignal DP hétérogène avec visibilité du matériel épidermique (flèche bleue). L’image de « pertuis » est également visible en regard du bord radial de la lésion (flèche jaune).
A npter un banal kyste mucoïde (étoile bleu) asymptomatique du 4ème axe.
L’ensemble de ces caractéristiques et le contexte clinique sont en faveur d’un kyste épidermoïde ou kyste d’inclusion épidermique.
Il s’agit d’une tumeur bénigne rare (<1% des tumeurs osseuses), correspondant à des ilôts intra-osseux de cellules épithéliales d’origine traumatique pour la localisation au niveau des doigts.
Le plus souvent asymptomatique, cette lésion peut être révélée par une douleur, une tuméfaction ou l’existence d’une odeur gênante du doigt en rapport avec la sécrétion de sébum.
L’aspect lacunaire centimétrique sans caractère d’aggressivité localisé en regard de la phalange distale est typique, avec une localisation plus fréquente au 3ème rayon.
Le traitement est chirurgical par résection-curetage.
1. Roth Sl. Squamous cysts involving the skull and distal phalanges. J Bone Joint Surg Am 1964 ; 46 : 1442-1450
2. Lussiez B, Le Nen D, Desbonnet P, et al. Le kyste épidermoïde intra-osseux phalangien : revue générale et description de deux cas. Ann Chir Main 1988 ; 7(4) : 305-9
Patient âgé de 33 ans, bilan de douleur du genou droit avec gonflement articulaire.
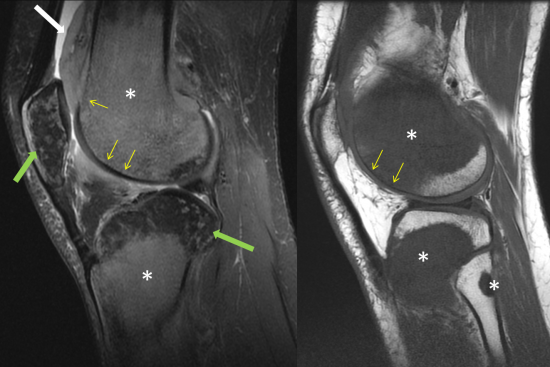
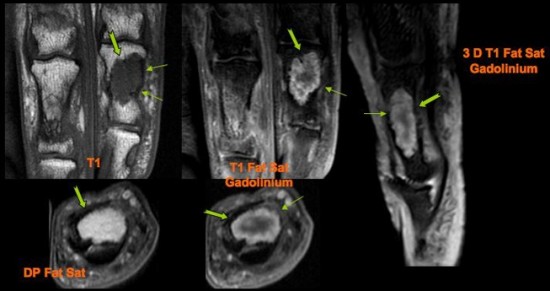
Fig1.: IRM du genou en coupes sagittales, DPFS et T1. Remplacement médullaire osseux métaphyso-épiphysaire de l'extrêmité distale du fémur et supérieure du tibia et de la tête de la fibula (étoile blanche) en franc hyposignal T1. Important envahissement des parties molles de la graisse sous-quadricipitale (flèche blanche). Respect relatif des corticales osseuses (petite flèche jaune). Oedème pommelé du spongieux de la patella et de l'épiphyse tibiale en hypersignal DPFS, sans traduction sur la séquence T1 (flèche verte).
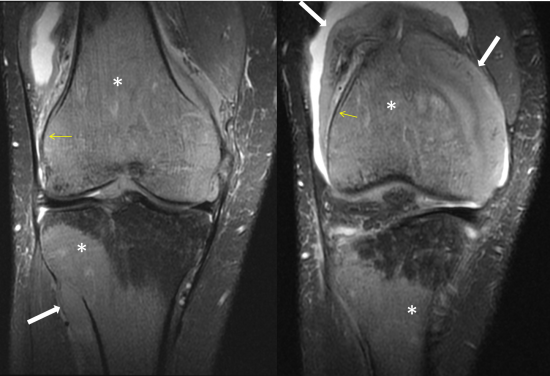
Fig.2: IRM du genou en coupes coronales, séquence DPFS. Remplacement médullaire osseux métaphyso-épiphysaire de l'extrêmité distale du fémur et supérieure du tibia et de la tête de la fibula (étoile blanche). Important envahissement des parties molles de la graisse sous-quadricipitale (flèche blanche). Respect relatif des corticales osseuses (petite flèche jaune).
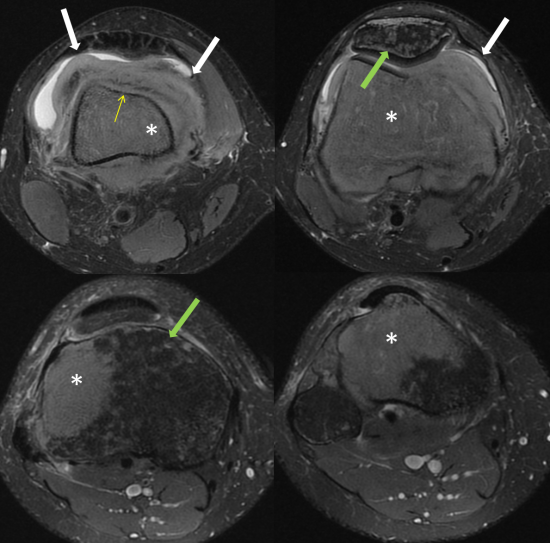
Fig3.: IRM du genou en coupes axiales, séquence DPFS. Remplacement médullaire osseux métaphyso-épiphysaire de l'extrêmité distale du fémur et supérieure du tibia et de la tête de la fibula (étoile blanche). Important envahissement des parties molles de la graisse sous-quadricipitale (flèche blanche). Respect relatif des corticales osseuses (petite flèche jaune). Oedème pommelé du spongieux de la patella et de l'épiphyse tibiale en hypersignal DPFS, sans traduction sur la séquence T1 (flèche verte).
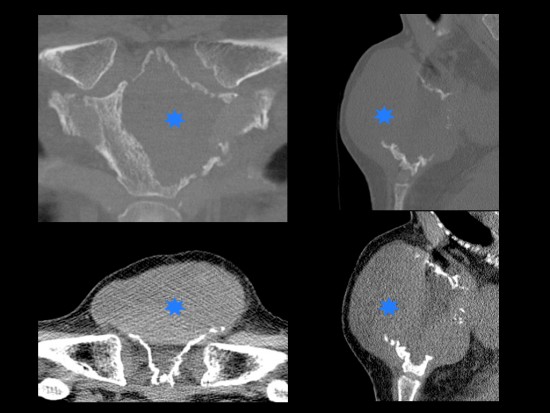
Bilan d'une tuméfaction sternale apparue en quelques semaines chez un homme de 44 ans.
Scanner: Syndrome de masse du manubrium sternal: matrice homogène non calcifiée avec lyse corticale et extension au niveau des parties molles.
Histologie: adénocarcinome rénal.
Cas d’un patient de 72 ans présentant une tumeur du rein droit (coupes axiales et coronales T1 avec saturation de la graisse et injection de gadolinium, figure 1) non métatastique avec thrombose de la veine rénale droite étendue à la veine cave inférieure (flèche blanche).
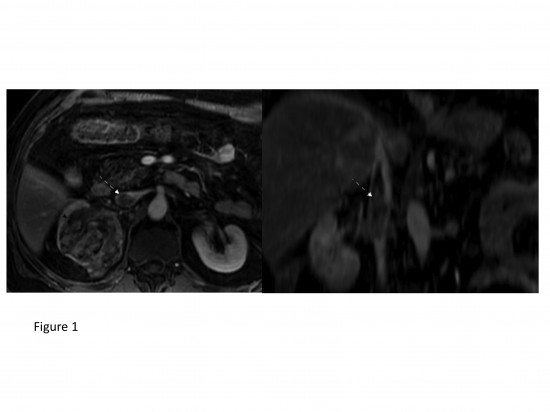
La résection chirurgicale est le traitement de référence pour les cancers du rein N0M0. Cependant, dans ce cas, la thrombose veineuse contre-indique la chirurgie du fait de l’important risque emboligène pulmonaire. Lors de la réunion pluridisciplinaire, il est décidé la mise en place par voie per-cutanée d'un filtre cave.
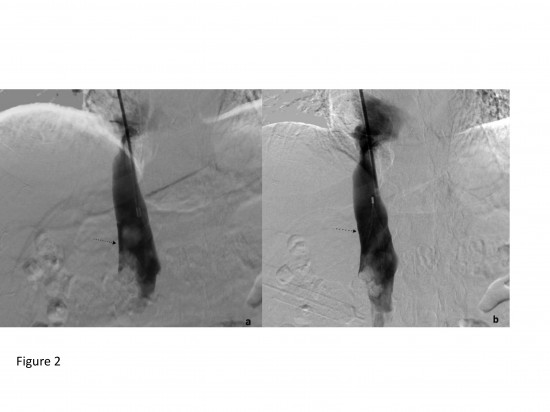
Une ponction de la veine jugulaire droite est réalisée ; dans un second temps, la cavographie (figure 2a) confirme la présence d’un thrombus de la veine rénale droite remontant au niveau de la veine cave inférieure (flèche noire). Le filtre est ensuite introduit entre l’abouchement de la veine cave dans l’oreillette droite et le thrombus avec une marge de sécurité de 2cm par rapport à celui-ci (b).
Dans le suivi réalisé à distance, il est mis en évidence une large lésion lytique agressive, centrée sur le col fémoral droit avec effraction corticale, envahissement des parties molles (figure 3) faisant évoquer dans le contexte une lésion secondaire rénale. 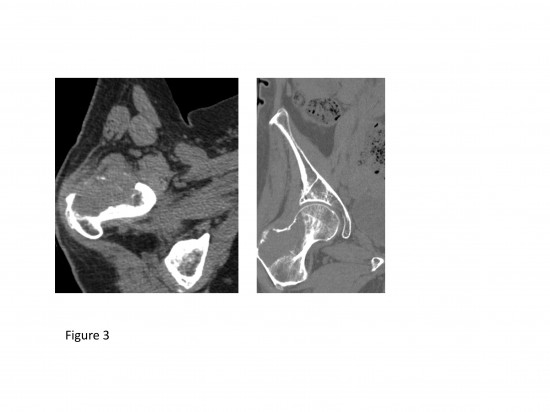
L’artériographie (figure 4) confirme le caractère nettement hypervasculaire caractéristique des métastases rénales ; l’embolisation thérapeutique est effectuée avant le traitement chirurgical (prothèse totale de hanche droite, figure 5) pour limiter le risque hémorragique per-opératoire.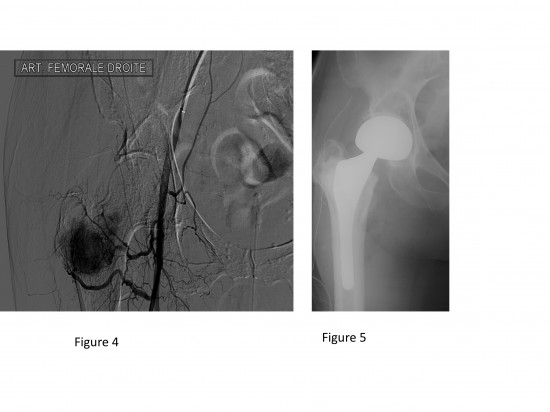
Remerciements aux Dr Cabral, Dr Perez, Dr Marcelin
REFERENCES
1.Harvey JJ, Hopkins J, McCafferty IJ, Jones RG. Inferior vena cava filters: What radiologists need to know. Clin Radiol. 2013 Feb 26
Bilan de douleurs chez un patient de 22 ans. TDM: lacune arrondie avec calcification centrale (tête de flèche blanche) et sclérose périphérique bien identiable. Il existe une densification trabéculaire et déformation périostée ainsi qu'une lyse corticale latérale (tête de flèche noire). Histologie post-opératoire: ostéoblastome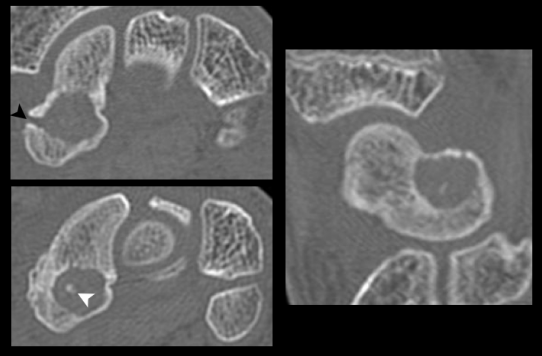
Jeune homme de 15 ans, découverte d’une lésion épiphysaire distale du fémur à la radiographie dans un contexte de gonalgies. Bilan complémentaire.
Figure 1. Scanner réalisé sans injection de produit de contraste, coupes axiales (A), coronales (B), sagittales (C). Lacune osseuse arrondie à bords nets, réguliers et lisses. Condensation dégressive périphérique d’allure inflammatoire. Absence de calcification centrale.
Figure 2. IRM pondérée en séquences DP-FatSat, en coupes axiales (A) et coronales (B). Lésion de signal central élévé, avec petit liseré d’hyposignal périphérique en rapport avec la condensation osseuse. Œdème du spongieux modéré en périphérie.
Figure 3. IRM avec séquences coronales T1 (A), coronales T1 après injection de chélates de gadolinium (B), séquences d’angio-MR 4D en coupes coronales (C) et séquences axiales T1 FatSat réalisées après injection. Réhaussement intense de la lacune osseuse (B,D), et cinétique de réhaussement artérielle (C).
Diagnostic: Ostéoblastome (preuve anatomo-pathologique)
Discussion:
Tumeur ostéogénique bénigne inflammatoire (3,5% des tumeurs primitives osseuses bénignes).
Le principal critère permettant de le différencier de l’ostéome ostéoïde est la taille (>20mm en cas d’ostéoblastome).
Aspect polymorphe des lésions en fonction de sa variation de taille, de sa minéralisation et de son agressivité locale.
Terrain: homme jeune d’âge entre 5 et 30 ans.
Localisation: rachis (27%) et os longs (fémur 12%, tibia 11%).
Il peut être de localisation métaphysaire (42%) , plus rarement diaphysaire (36%) et épiphysaire (22%).
Localisation corticale (65%), spongieuse (35%) ou sous-périostée (5%).
Au rachis, il atteint le plus souvent l’arc postérieur.
Il existe un polymorphisme marqué des ostéoblastomes.
-aspect d’ostéome ostéoïde « géant » (comme dans le cas présent), avec un nidus plus inconstant
-lésion soufflante simulant un kyste anévrysmal
-aspect ostéolytique avec rupture de corticale, simulant une tumeur maligne
-lésion condensante.
Diagnostics différentiels: ostéome ostéoïde, chondroblastome, ostéosarcome, kyste anévrysmal, dysplasie fibreuse, chondrosarcome, ostéomyélite, tumeur à cellules géantes et sarcome d’Ewing.
Références:
Tumeurs osseuses et pseudo-tumeurs osseuses, imagerie rhumatologique et orthopédique, Laredo et al.
Lombaire d’horaire inflammatoire chez un jeune homme de 21 ans.
IRM du rachis lombaire (a : sagittal T1, b : sagittal T2 STIR, c : coronal oblique T2 STIR, axial T2)
Net œdème du spongieux en hypersignal T2 et hyposignal T1 intéressant l'ensemble du pédicule gauche de L5, avec extension corporéale postéro-latérale gauche. Cet oedème est centré par une petite lésion ovalaire qui apparaît en hyposignal T1 et T2, bien limitée, intéressant la partie la plus latérale du pédicule.
Scanner du rachis lombaire en fenêtre osseuse (a: sagittal, b: coronal, c: axial) : Nidus ossifié mesurant 7mm en antéro-postérieur, bien limité, associé à une nette sclérose périphérique et ébauche d’ossification de la partie latérale de l’annulus fibrosus adjacent.
Exostose à large base d'implantation de la région métaphyso-diaphysaire fémorale distale (flèches blanches). La coiffe cartilagineuse apparaît régulière avec une épaisseur moyenne inférieure à 10 mm (petites flèches blanches).
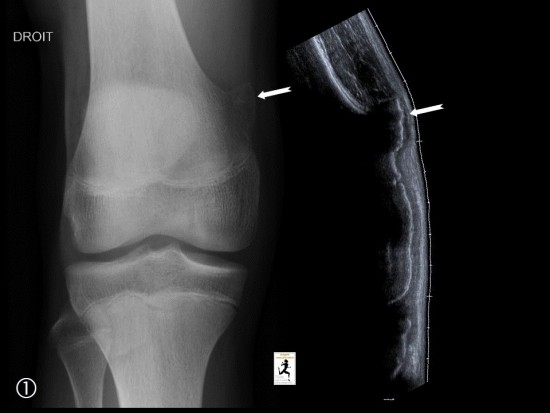
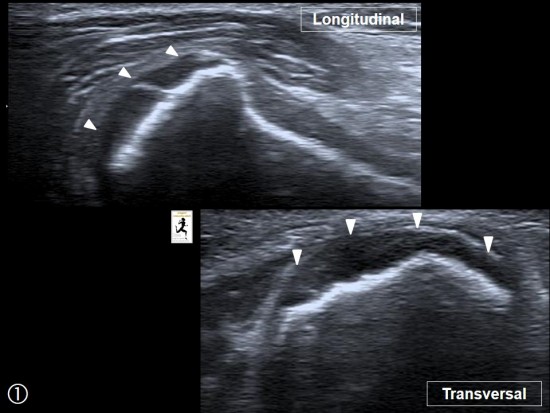
Enfant de 16 ans présentant un "accrochage" scapulaire ancien ainsi qu'un décollement du bord médial de la scapula (ne se majorant pas lors des mouvements).
Scanner: image d'addition pédiculée avec matrice osétochondrale à bords réguliers en continuité avec la corticale et la matrice de la scapula évocatrice d'ostéochondrome (ou exostose).
Pas de bursite serratothoracique ou serratoscapulaire associée.
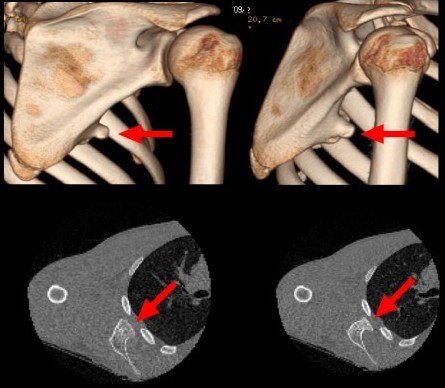
Les autres causes de snapping scapula sont:
- au niveau des structures osseuses: hypertrophie du tubercule de Luschka, cals osseux, scoliose ou cyphose thoracique
- au niveau des parties molles: élastofibrome dorsal, bursite scapulothoracique, bandelettes fibreuses.
Des associations ont été décrites entre snapping scapula et syndrome de la traversée cervicothoracobrachiale: le diagnostic de snapping scapula doit être évoqué en cas d'échec de résection de la première côte.
En cas d'atteinte du muscle grand dentelé ou du nerf thoracique long, le décollement du versant médial de la scapula se majore lors des mouvements.
Le traitement peut être médical ou chirurgical.
Découverte fortuite d'une mélorhéostose du 2ème métatarsien du pied droit.
Radiographie des pieds de face: Epaissisement cortical avec condensation intra-médullaire du 2ème métatarsien.
Scanner du pied droit en fenêtre osseuse (a : coronal, b : sagittal, c : axial) : Epaississement cortical avec condensation intra-médullaire du 2ème métatarsien.
La mélorhéostose est une dysplasie rare caractérisée par une hyperostose en « coulée de bougie », très particulière par sa distribution selon un ou plusieurs sclérotome, qui serait due à un trouble de l’ossification endochondrale et membranaire. Elle est sporadique sans caractère héréditaire ni prépondérance de sexe.
Clinique :
- souvent asymptomatique, elle peut être découverte de façon fortuite ou après une fracture.
- Dans 1/3 des cas elle s’accompagne de douleur et raideur articulaire.
- Chez l’enfant on peut observer une raideur articulaire ou des anomalies de croissance d’un membre qui est raccourci, allongé, incurvé et augmenté de volume.
Imagerie :
- Hyperostose corticale compacte, en coulée de bougie, développée à la surface de la diaphyse des os longs +/- associée à une hyperostose endostée et une oblitération de la cavité médullaire.
- Siège sur un versant (latéral ou médial ) du membre, franchissant les articulations.
- Distribution monostotique ou polyostotique et suit un ou plusieurs sclérotomes.
- La coulée peut être associée à une masse des tissus mous, intramusculaire, constituée d’os et de cartilage, dans le territoire musculaire correspondant au sclérotome atteint.
- L’IRM montre un hyposignal en T1 et en T2.
Imagerie rhumatologique et orthopédique; tumeurs osseuses et pseudo-tumeurs osseuses, Laredo
Enfant de 7 ans présentant des douleurs inflammatoires de la hanche gauche.
IRM: image arrondie cervico-diaphysaire en hypersignal T2 de topographie strictement corticale et correspondant au nidus (flèche rouge). Décollement périosté associé (flèche bleue). Oedème médullaire (flèches vertes) et de la face profonde du muscle ilio-psoas (flèche jaune).
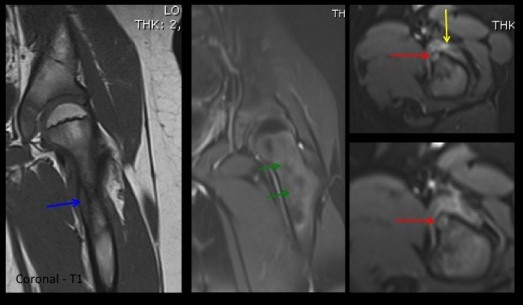
Bilan radiographique normal.
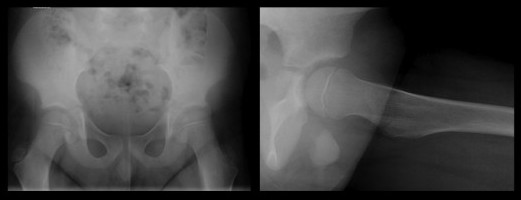
Clichés du Dr Sébastien Brunot.
Patiente de 24 ans adressée pour bilan cartilagineux et labral dans le cadre de douleurs de la hanche gauche.
Arthro TDM de la hanche gauche :
Images (a) coupe axiale, (b) coupe coronale et (c) coupe sagittale : Image lacunaire centimétrique de la partie antérieure du cotyle gauche, contenant une calcification centrale (flèche bleue). Il s'y associe une condensation périphérique progressivement dégressive vers l'os normal (type 1A2), évoquant une lacune inflammatoire.
IRM des hanches :
Images (d) et (e) : Coupes axiales pondérées DP SPIR : Hypersignal inflammatoire du cotyle gauche (flèche verte) entourant une petite image corticale en hyposignal (flèche orange).
Images (f) et (g) : Coupes coronales pondérées DP SPIR : Hypersignal inflammatoire du cotyle gauche extensif aux parties molles adjacentes (flèche verte).
Images (h) et (i) : Coupes coronales pondérées T1 : Hyposignal modéré du cotyle gauche en rapport avec l'oedème inflammatoire (flèche verte) situé au pourtour d'un petit hyposignal cortical marqué (flèche orange).
Ce cas illustre un ostéome ostéoïde du cotyle gauche, expliquant les douleurs de la patiente.
Il s'agit d'une tumeur bénigne assez fréquente (15% des tumeurs osseuses bénignes) de la personne jeune (5-30 ans). Elle se présente habituellement par des douleurs à recrudescence nocturne calmées par l'aspirine. Il affecte le plus souvent les os longs (fémur et tibia) mais également le rachis et les os plats. Il est le plus souvent de topographie diaphysaire et corticale.
Sur le plan thérapeutique, des traitements percutanés peuvent être proposés en première intention (radiofréquence, photocoagulation au laser, alcoolisation et éxérèse percutanée). L'éxérèse chirurgicale est proposée en deuxième intention.
J Med Case Rep. 2016 Aug 24;10(1):232. doi: 10.1186/s13256-016-1016-2.
J Med Case Rep. 2016 Dec 3;10(1):348.
Patiente de 19 ans présentant des douleurs chroniques nocturnes de l'extrémité supérieure du tibia sensibles au traitement par aspirine.
TDM: présence d'un nidus (![]() ) hyperdense entouré dun fin liseré hypodense. Sclérose périphérique (
) hyperdense entouré dun fin liseré hypodense. Sclérose périphérique (![]() ).
).
IRM: nidus (![]() ) en hyposignal T1 sans et après injection de gadolinium et en T2.
) en hyposignal T1 sans et après injection de gadolinium et en T2.
Oedème réactionnel en hypersignal T2. Sclérose périphérique (![]() ) en hyposignal T1 et T2.
) en hyposignal T1 et T2.
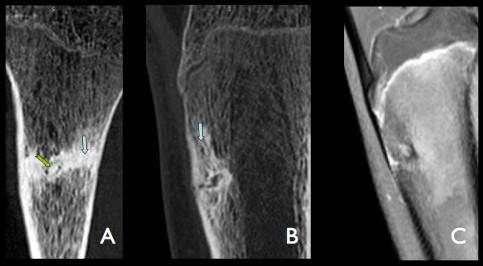
A: TDM coupe coronale. B: TDM coupe sagittale C: IRM DP FS coupe sagittale
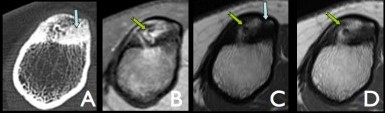
A: TDM coupe axiale B: IRM axial DP FS C: IRM: axial T1 D: axial T1 gado
Douleurs persistantes chez un homme de 18 ans depuis environ un an en regard de l’épine iliaque antéro-inférieure droite, notamment nocturnes et insomniantes, répondant aux AINS (anti-inflammatoires non stéroïdiens). 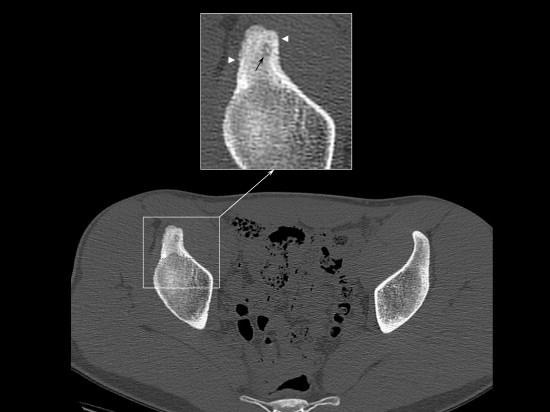
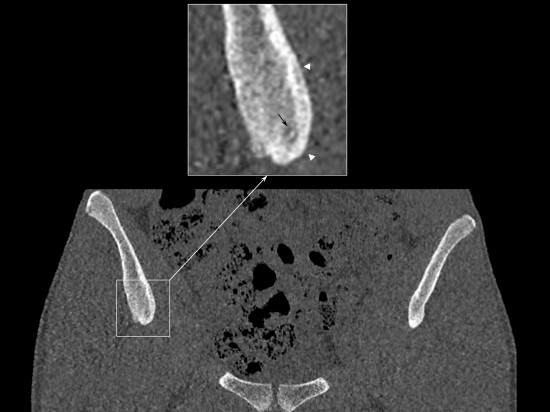
Le scanner réalisé met en évidence une plage d’ostéocondensation médullaire centrée sur l’épine iliaque antéro-inférieure (ostéosclérose délimitée par la ligne noire en pointillée).Il s’y associe un épaississement cortical régional, secondaire à des appositions périostées chroniques incorporées (ou lamellaires en voie d’incorporation) : têtes de flèches blanches. Ces remaniements osseux sont à l’origine d’un épaississement de la structure osseuse dans la région de l’EIAI droite, bien visible en comparaison du côté sain controlatéral.
Enfin, présence d’une lacune ostéolytique ovalaire du spongieux de 6 mm, à contours nets, centrée sur cette plage d’ostéosclérose présentant un aspect en cocarde avec une hyperdensité punctiforme centrale (flèche noire).
Devant l’ensemble du tableau clinico-radiologique, on pose le diagnostique d’ostéome ostéoïde intraspongieux iliaque.
Sur le plan topographique, les classifications récentes (basées sur l’analyse IRM ou TDM) distinguent quatre formes : Intracorticale (36 %), Sous-périostée (28 %), Endostée (20%) et Intraspongieuse (16%).
Selon certains auteurs, les formes intramédullaires et intracorticales correspondraient en fait à une "migration" en profondeur d'une lésion initialement d'origine souspériostée. Cette "migration" serait secondaire au remodelage osseux, avec appositions périostées, épaississement cortical et érosion endostée (Kayser and al.)
Ci-dessous un schéma des différentes localisations d'OO en fonction de la corticale native sur une coupe d'un os long : A = Sous-périostée, le nidus (disque gris) est situé à la surface externe de la corticale, en continuité avec le périoste (A1). Dans la majorité des cas, il s'y associe des remaniements osseux avec appositions périostées, le nidus sous-periostée apparaissant alors "enterré" sous l'épaississement cortical (A2). B = Intracorticale, dans l'éapisseur de la corticale native. C = Endostée et D = Intramédullaire, le nidus est alors fréquemment entouré d'une sclérose du spongieux (non représentée sur le schéma). 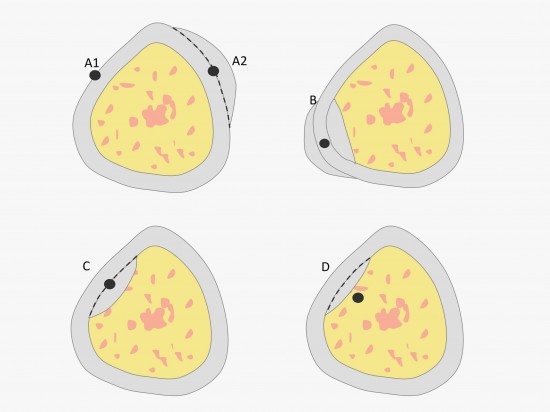
DISCUSSION
L’Ostéome Ostéoïde (OO) est une tumeur fréquente (représentant 4% des tumeurs osseuses primitives et 15 % des tumeurs osseuses bénignes) essentiellement observée entre 7 et 25 ans, avec prédominance masculine (sex-ratio=3/1).
Le mode de révélation classique est l’apparition progressive de douleurs modérées à prédominance nocturnes avec une bonne réponse aux AINS dans 70% des cas, ce qui constitue un élément diagnostique évocateur (la symptomatologie étant secondaire à l’effet vasodilatateur des prostaglandines concentrées dans le nidus, expliquant l’efficacité spécifique des AINS).
TOPOGRAPHIE
L’OO affecte les os longs dans près de 75% des cas (généralement de siège diaphysaire), notamment au membre inférieur (60% des cas). Le rachis (arc postérieur) est une atteinte classique, comme les os du carpe ou du tarse (en tout 30% des cas). L’atteinte des os plats est plus rare.
IMAGERIE
La caractéristique radiologique principale est la présence d’une tumeur de petite taille (appelée « nidus ») généralement infracentimétrique contrastant avec l’importance de la réaction osseuse spongieuse et corticale régionale, plus facilement mise en évidence que le nidus lui-même et faisant de l’OO la principale tumeur osseuse bénigne dite « inflammatoire ».
Le nidus se caractérise en radiographie et scanner par une lacune osseuse ovalaire infracentimétrique avec typiquement une calcification punctiforme centrale lui conférant un aspect en cocarde. Le nidus est en pratique parfois difficilement mis en évidence sur les radiographies, la réaction corticale associée pouvant le masquer selon l’incidence.
La réaction osseuse régionale est en revanche facilement mise en évidence, se caractérisant par une ostéocondensation médullaire et un épaississement cortical secondaire à des appostions périostées chroniques incroporées (ou lamellaires en voie d’incorporation lorsqu’elles sont subaigues).
REFERENCES
Morphologic changes of osteoid osteoma at CT. Tourraine S. and al.Radiology, 2014
Imagerie musculosquelettique, Pathologies générales. Anne Cotten - 2ème édition, 2013.
Jeune Homme de 22 ans présentant une limitation douloureuse des mouvements de flexion-extension sans notion de traumatisme. Bilan radiographique (hors centre) non connu.
Sur l'examen tomodensitométrique, la face dorsale du Capitatum est le siège d'une lésion annulaire sclérotique (flèche blanche) centrée par un nidus contenant une calcification mieux visualisée à l'IRM (petite flèche jaune).
Le Capitataum présente un oedème de la médullaire osseuse (tête de flèche blanche). Il s'y assosie une synovite dorsale majeure (petites flèches blanches) se rehaussant de façon intense après injection de Gadolinium
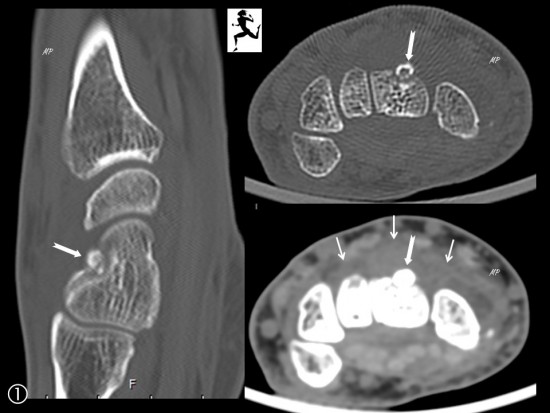
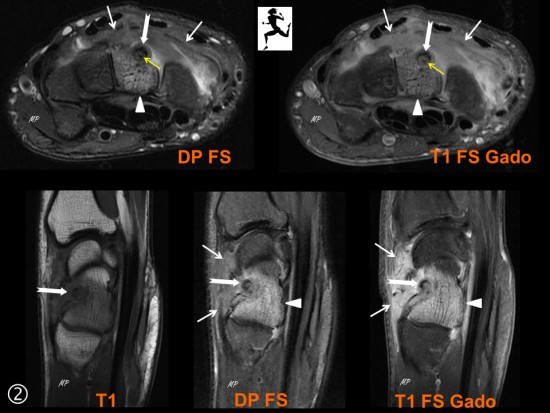
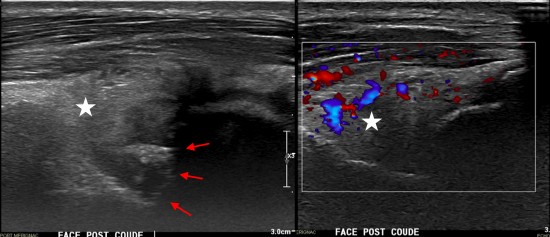
Patient adressé pour bilan de douleurs postérieurs du coude avant injection de PRP.
L'échographie réalisée dans un premier temps visualise une synovite postérieure franchement hyperhémique en doppler couleur (étoile blanche), associée à un aspect remanié de la face postérieure de l'extrémité inférieure de l'humérus (étoile blanche), associée à un aspect remanié de la face postérieure de l'extrémité inférieure de l'humérus (flèches rouges).
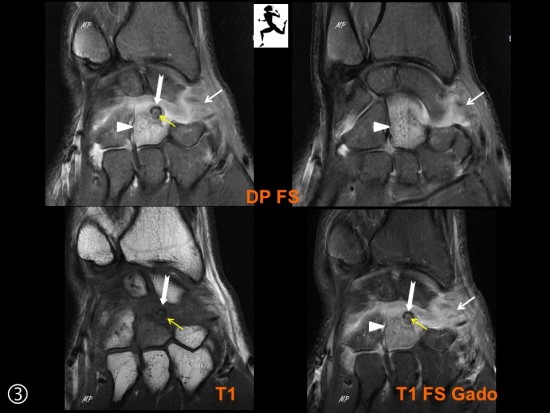
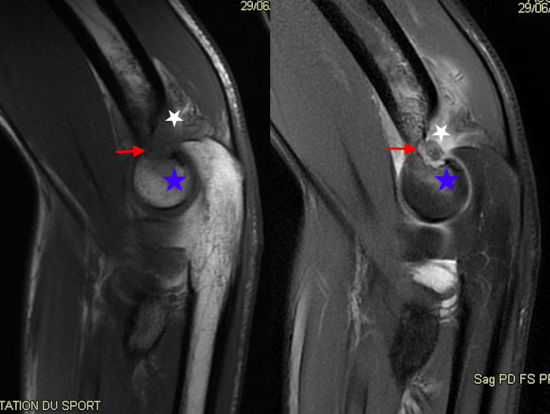
L'IRM réalisée dans un second temps (sagital T1 et DP FatSat) retrouve la synovite postérieure (étoile blanche), associée à un oedème médullaire de l'extrémité distale de l'humérus (étoile bleu), centrée sur une lésion nodulaire juxta-corticale extra osseuse (flèche rouge) faisant suspecter un ostéome ostéoïde sous périosté.
Le scanner réalisé dans les suites confirme le diagnostic montrant une lésion annulaie sclérotique (flèche rouge) centrée par un nidus contenant une calcification de la face psotérieure de la fossette olécranienne de l'humérus.
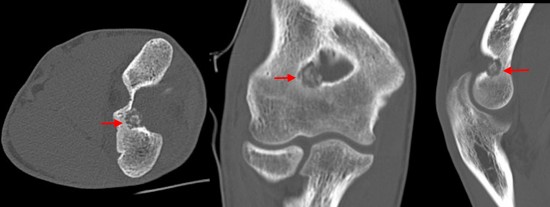
Du fait du caractère articulaire de la lésion, un traitement médical par biphosphonate apparait iniqué en première intention plutôt qu'une thermo-ablation percutanée d'emblée.
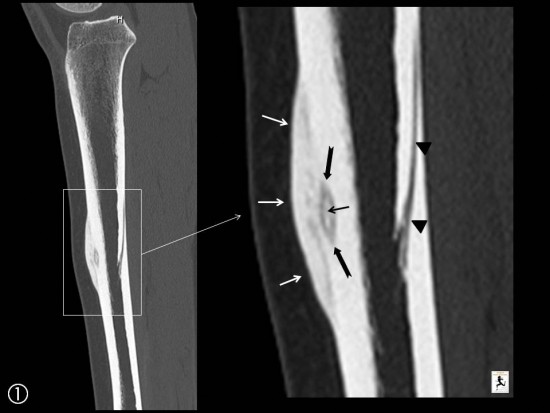
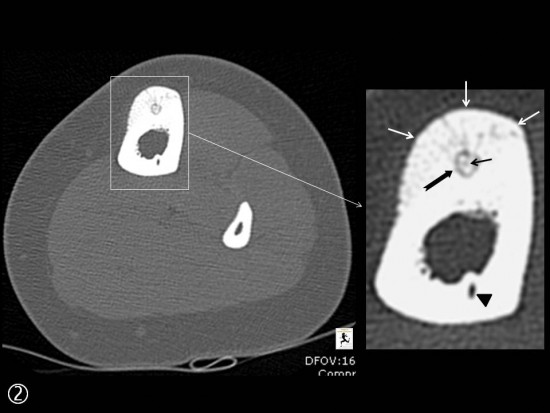
Tuméfaction sensible du tiers moyen de la crête tibiale chez une jeune patiente de 15 ans évoluant depuis plusieurs mois.
Sur le scanner, lacune de la corticale tibiale antérieure correspondant au nidus (flèches noires) avec calcification centrale (petites flèches noires), ostéosclérose de voisinage et aposition périostée (petites flèches blanches).
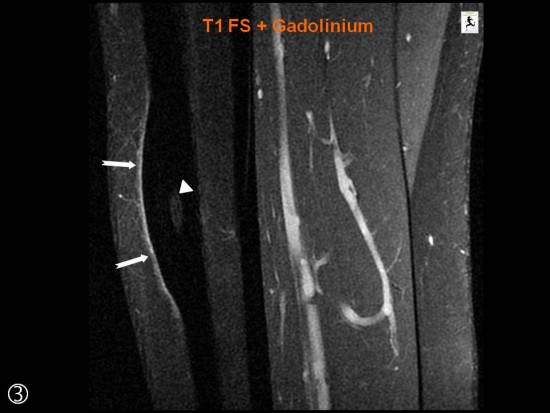
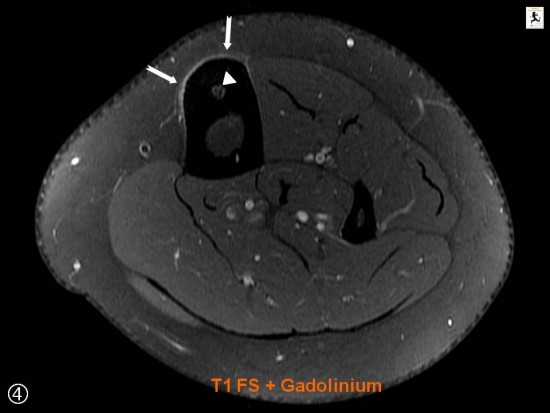
Sur l'IRM les remaniements inflammatoires sont minimes avec uniquement prise de contraste périostée en regard de la lésion (flèches blanches). Nidus (têtes de flèche blanches)
Canal nouricier au sein de la corticale postérieure (têtes de flèche noires).